Carboidratos: Principais Fornecedores de Energia
No momento em que você está lendo estas linhas e procurando entender o seu conteúdo, suas células nervosas estão realizando um trabalho e, para isso, utilizam a energia que foi liberada a partir da oxidação de moléculas de um carboidrato chamado glicose.
Classificação dos carboidratos
Uma classificação simplificada dos carboidratos, ou glicídios, consiste em dividi-los e três categorias principais: monossacarídeos, oligossacarídeos e polissacarídeos.
Monossacarídeos: os mais simples
Os monossacarídeos são carboidratos simples, de formula molecular (CH2O)n, onde n é no mínimo 3 e no máximo 8. São os verdadeiros açucares, solúveis em água e, de modo geral, de sabor adocicado. Os de menor número de átomos de carbono são as trioses (contêm três átomos de carbono). Os biologicamente mais conhecidos são os formados por cinco átomos de carbonos (chamados de pentoses) e os formados por seis átomos de carbono (hexoses).
Na tabela abaixo você encontra as hexoses e pentoses mais conhecidas, seus papeis biológicos e as fontes de obtenção. Não se preocupem com as fórmulas moleculares, fixem-se apenas as fontes onde são encontradas os açucares e seu papel biológico.
Pentose | |
Ribose | Desoxirribose |
Papel Biológico | Papel Biológico |
Matéria-prima para a fabricação do ácido nucléico RNA. Fórmula molecular: C5H10O5 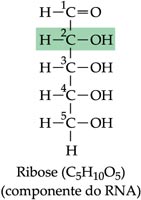 | Matéria-prima para a fabricação do ácido nucléico DNA. Fórmula molecular: C5H10O4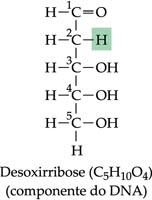 |
Hexose | ||
Glicose | Frutose | Galactose |
 |  |  |
Papel Biológico | Papel Biológico | Papel Biológico |
Principal fornecedor de energia para o trabalho celular. É a base para a formação da maioria dos carboidratos mais complexos. Produzida na fotossíntese pelos vegetais. Encontrada no sangu, no mel e nos tecidos dos vegetais. Fórmula molecular: C6H12O6 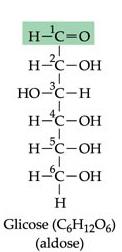 | Também fornece energia para a célula. Encontrada principalmente em frutos doces e também no esperma humano. Fórmula molecular: C6H12O6 | Papel energético. Encontrada no leite, como componente do dissacarídeo lactose. Fórmula molecular: C6H12O6 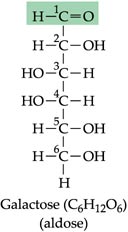 |
Oligossacarídeos: nem tão simples, nem tão complexos
Oligossacarídeos são açucares, formados pela união de dois a seis monossacarídeos, geralmente hexoses. O prefixo oligo deriva do grego e quer dizer pouco. Os oligossacarídeos mais importantes são os dissacarídeos.

Açucares formados pela união de duas unidades de monossacarídeos, como, por exemplo, sacarose, lactose e maltose. São solúveis em água e possuem sabor adocicado. Para a formação de um dissacarídeo , ocorre reação entre dois monossacarídeos, havendo liberação de uma molécula de água. É comum utilizar o termo de desidratação intermolecular para esse tipo de reação, em que resulta uma molécula de água durante a formação de um composto originado a partir de dois outros.
Veja o caso do dissacarídeo sacarose, que é o açúcar mais utilizado para o preparo de doces, sorvetes, para adoçar refrigerantes não dietéticos e o “cafezinho”. Sua fórmula molecular é C12H22O11. Esse açúcar é resultado da união de uma frutose e uma glicose. Como foi visto na tabela anterior, tanto a glicose como a frutose possuem a fórmula molecular C6H12O6. Como ocorre a liberação de uma molécula de água para a formação de sacarose, a sua fórmula molecular possui dois hidrogênios e um oxigênio a menos.
Dissacarídeo | Constituição | Papel biológico | Fontes |
Sacarose | glicose-frutose | energético | cana-de-açucar, beterraba e rapadura |
Lactose | glicose-galactose | energético | leite |
Polissacarídeos: os mais complexos
Como o nome sugere (poli é um termo derivado do grego e quer dizer muitos), os polissacarídeos são compostos macromoleculares (moléculas gigantes), formadas pela união de muitos (centenas) monossacarídeos. Os três polissacarídeos mais conhecidos dos seres vivos são amido, glicogênio e celulose.
Ao contrário da glicose, os polissacarídeos dela derivados não possuem sabor doce, nem são solúveis em água.
Polissacarídeo | O que é importante saber |
Amido  | É um polissacarídeo de reserva energética dos vegetais. As batatas, arroz e a mandioca estão repletos de amido, armazenado pelo vegetal e consumido em épocas desfavoráveis pela planta. O homem soube aproveitar essas características e passou a cultivar os vegetais produtores de amido. Os pães e bolos que comemos são feitos com farinha de trigo, rica em amido. Lembrem-se que para o amido ser aproveitado pelo nosso organismo, é preciso digeri-lo, o que ocorre primeiramente na boca e depois no intestino, com adição de água e a participação de catalisadores orgânicos, isto é, substâncias que favorecem ou aceleram as reações químicas. |
Glicogênio 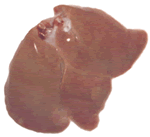 | É um polissacarídeo de reserva energética dos animais; portanto, equivalente ao amido dos vegetais. No nosso organismo, a síntese de glicogênio ocorre no fígado, a partir de moléculas de glicose. Logo, fígado de boi e fígado de galinha são alimentos ricos em glicogênio. |
Celulose  | É o polissacarídeo de papel estrutural, isto é, participa da parede das células vegetais. Poucos seres vivos conseguem digeri-lo, entre eles alguns microrganismos que habitam o tubo digestivo de certos insetos (cupins) e o dos ruminantes (bois, cabras, ovelhas, veados etc.). |
Lipídios: Serão eles vilões?

As duas substâncias mais conhecidas dessa categoria orgânica são as gorduras e os óleos. Se por um lado, esses dois tipos de lipídios preocupam muitas pessoas por estarem associadas a altos índices de colesterol no sangue, por outro, eles exercem importantes funções no metabolismo e são fundamentais para a sobrevivência da maioria dos seres vivos. Um dos papéis dos lipídeos é o de funcionar como eficiente reserva energética. Ao serem oxidados nas células, geram praticamente o dobro da quantidade de calorias liberadas na oxidação de igual quantidade de carboidratos. outro papel dos lipídios é o de atuar como eficiente isolante térmico, notadamente nos animais que vivem em regiões frias. Depósitos de gordura favorecem a flutuação em meio aquático; os lipídios são menos densos que a água.

Além desses dois tipos fundamentais de lipídios, existem outros que devem ser lembrados pelas funções que exercem nos seres vivos. São as ceras, os fosfolipídios, os esteróides, as prostaglandinas e os terpenos.
 | as ceras existem na superfície das folhas dos vegetais e nos esqueletos de muitos animais invertebrados (por exemplo, os insetos e os carrapatos) funcionam como material impermeabilizante. Não devemos esquecer dos depósitos de cera que se formam nas nossas orelhas externas como função protetora; |
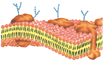 | os fosfolipídios são importantes componentes das membranas biológicas (membrana plasmática e de muitas organelas celulares); |
 | os esteróides são lipídeos que atuam como reguladores de atividades biológicos; |
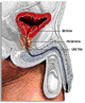 | as prostaglandinas atuam como mensageiros químicos nos tecidos de vertebrados; |
 | os terpenos estão presentes em alguns pigmentos de importância biológica, como a clorofila e os carotenóides. |
Como são os lipídios?
 | Os lipídios são compostos orgânicos insolúveis em água. Dissolvem-se bem em solventes orgânicos como o éter e o álcool. A estrutura química molecular dos lipídios é muito variável. Vamos dar a você uma noção da composição química de óleos e gorduras e alguns dos principais componentes desse grupo. |
Óleos e gorduras – pertencem à categoria dos ésteres e são formados por meio da reação de um álcool, chamado glicerol, com ácidos orgânicos de cadeia longa, conhecidos como ácidos graxos. A exemplo do que ocorre com os carboidratos, a reação do glicerol com os ácidos graxos é de condensação, havendo liberação de moléculas de água.
Como o glicerol é um triálcool (possui três terminações OH na molécula), três ácidos graxos a ele se ligam, formando-se o chamado triglicerídeos. Nos seres vivos, existem diversos tipos de triglicerídeos, uma vez que são muitos os tipos de ácidos graxos deles participantes.
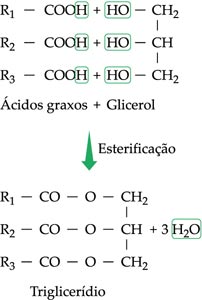
Como o glicerol é um triálcool (possui três terminações OH na molécula), três ácidos graxos a ele se ligam, formando-se o chamado triglicerídeos. Nos seres vivos, existem diversos tipos de triglicerídeos, uma vez que são muitos os tipos de ácidos graxos deles participantes.

Com relação aos ácidos graxos que participam de um triglicerídeos, lembre-se que são substâncias de cadeia longa. Em uma das extremidades de cada ácido graxo há uma porção ácida (a “cabeça”), seguida de uma longa “cauda” formada por uma seqüência de átomos de carbono ligados a átomos de hidrogênio.
Nos chamados ácidos graxos saturados, todas as ligações disponíveis dos átomos de carbono são ocupados por átomos de hidrogênio. Já nos ácidos graxos insaturados, nem todas as ligações do carbono são ocupadas por hidrogênios; em conseqüência, forma-se o que em química é conhecido como duplas ligação entre um átomo de carbono e o seguinte (motivo pelo qual o ácido graxo recebe a denominação de insaturado). Nos ácidos graxos poliinsaturados há mais de uma dupla ligação.
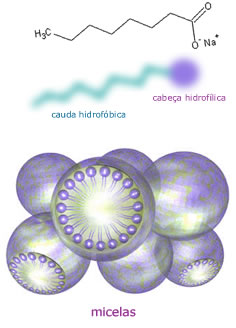
Fosfolipídios – as membranas biológicas são constituídas por fosfolipídios. Nos fosfolipídios há apenas duas moléculas de ácidos graxos – de natureza apolar – ligadas ao glicerol. O terceiro componente que se liga ao glicerol é um grupo fosfato (daí a denominação fosfolipídio) que, por sua vez, pode estar ligado a outras moléculas orgânicas. Assim, cada fosfolipídio contém uma porção hidrofóbica – representada pelos ácidos graxos – e uma porção hidrofílica – corresponde ao grupo fosfato e às moléculas a ele associadas. Um fato notável é que, ao serem colocadas em água, as moléculas de fosfolipídios podem assumir o formato de um esfera, conhecida como micela: as porções polares, hidrofílicas, distribuem-se na periferia , enquanto as caudas hidrofóbicas ficam no interior da micelas afastadas da água.
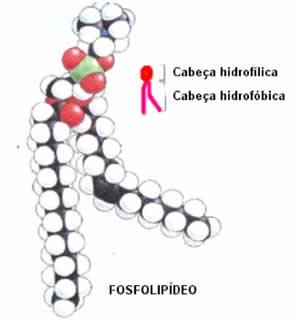
Nas células, os fosfolipídios das membranas biológicas (membrana plasmática e de muitas organelas) dispõem-se formando bicamadas. As porções hidrofílicas ficam em contato com a água dos meios interno e externo celular, enquanto as hidrofóbicas situam-se internamente na membrana, afastadas da água, o que faz lembrar um sanduíche de pão-de-forma.
Prostaglandinas – essas substâncias atuam como mensageiras químicas em muitos tecidos humanos. Seu nome deriva do fato de terem sido descobertas em componentes do sêmen humano produzidos na glândula próstata.
Terpenos – lipídios de cadeia longa, componentes de pigmentos biologicamente importantes como a clorofila (pigmento vegetal participante da fotossíntese). Uma importante categoria de terpenos é a dos carotenóides (pigmentos amarelados), dos quais o mais importante é o B-caroteno (encontrado em muitos alimentos de origem vegetal, como a cenoura, por exemplo), que é precursor da vitamina A (retinol).
Esteróides – alguns esteróides são hormônios (por exemplo, a testosterona, o hormônio sexual masculino) e outros são vitaminas (por exemplo, a vitamina D). O colesterol, que para os químicos é um álcool complexo, é outro exemplo de esteróide: é importante componente de membranas celulares, embora hoje seja temido como causador de obstrução (entupimento) em artérias do coração.
O colesterol não “anda” sozinho no sangue. Ele se liga a uma proteína e, dessa forma, é transportado. Há dois tipos principais de combinações: o HDL, que é o bom colesterol e o LDL que é o mau colesterol. Essas siglas derivam do inglês e significam lipoproteína de alta densidade (HDL – High Density Lipoprotein) e lipoproteína de baixa densidade (LDL – Low Density Lipoprotein).
O LDL transporta colesterol para diversos tecidos e também para as artérias, onde é depositado, formando placas que dificultam a circulação do sangue, daí a denominação mau colesterol. Já o HDL faz exatamente o contrário, isto é, transporta colesterol das artérias principalmente para o fígado, onde ele é inativado e excretado como sais biliares, justificando o termo bom colesterol.
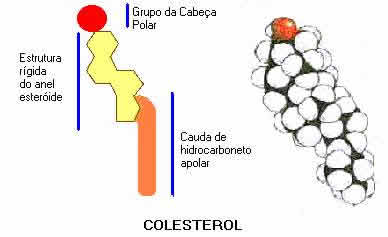
O colesterol não existe em vegetais, o que não significa que devemos abusar dos óleos vegetais, porque afinal, a partir deles (ácidos graxos), nosso organismo produz colesterol.
Proteínas: A construção dos seres vivos
Você já deve ter ouvido falar de proteínas, certo? As proteínas são compostos orgânicos relacionados ao metabolismo de construção. Durante as fases de crescimento e desenvolvimento do indivíduo, há um aumento extraordinário do número de suas células passam a exercer funções especializadas, gerando tecidos e órgãos.
As proteínas possuem um papel fundamental no crescimento, já que muitas delas desempenham papel estrutural nas células, isto é, são componentes da membrana plasmática, das organelas dotadas de membrana, do citoesqueleto dos cromossomos etc. E para produzir mais células é preciso mais proteína. Sem elas não há crescimento normal. A diferenciação e a realização de diversas reações químicas componentes do metabolismo celular dependem da paralisação de diversas reações químicas componentes do metabolismo celular dependem da participação de enzimas , uma categoria de proteínas de defesa, chamadas anticorpos. Sem eles, nosso organismo fica extremamente vulnerável.

Certos hormônios, substâncias reguladoras das atividades do nosso organismo, também são protéicos. É o caso da insulina, que controla a taxa de glicose sangüínea.
As proteínas são macromoléculas formadas por uma sucessão de moléculas menores conhecidas como aminoácidos. A maioria dos seres vivos, incluindo o homem, utiliza somente cerca de vinte tipos diferentes de aminoácidos, para a construção de suas proteínas. Com eles, cada ser vivo é capaz de produzir centenas de proteínas diferentes e de tamanho variável.
Como é isso possível, a partir de um pequeno número de aminoácidos?
Imagine um brinquedo formado por peças de plástico, encaixáveis umas nas outras, sendo as cores em número de vinte, diferentes entre si. Havendo muitas peças de cada cor, como você procederia para montar várias seqüências de peças de maneira que cada seqüência fosse diferente da anterior? Provavelmente , você repetiria as cores, alternaria muitas delas, enfim, certamente inúmeras seriam as seqüências e todas diferentes entre si. O mesmo raciocínio é valido para a formação das diferentes proteínas de um ser vivo, a partir de um conjunto de vinte aminoácidos.
Cada aminoácido é diferente de outro. No entanto, todos possuem alguns componentes comuns. Todo aminoácido possui um átomo de carbono, ao qual estão ligados uma carboxila, uma amina e um hidrogênio. A quarta ligação é a porção variável, representada por R, e pode ser ocupada por um hidrogênio, ou por um metil ou por outro radical.
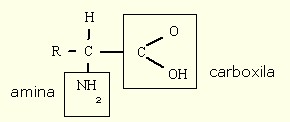
Ligação peptídica: unindo aminoácidos
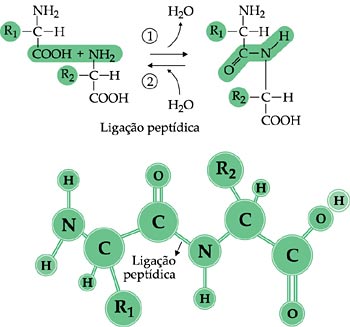 | Do mesmo modo que em um trem cada vagão está engatado ao seguinte, em uma proteína cada aminoácido está ligado a outro por uma ligação peptídica. Por meio dessa ligação, o grupo amina de um aminoácido une-se ao grupo carboxila do outro, havendo a liberação de uma molécula de água. Os dois aminoácidos unidos formam um dipeptídio. A ligação de um terceiro aminoácido ao dipeptídeo origina um tripeptídeo que então, contém duas ligações peptídicas. Se um quarto aminoácido se ligar aos três anteriores, teremos um tetrapeptídeo, com três ligações peptídicas. Com o aumento do número de aminoácidos na cadeia, forma-se um polipetídio, denominação utilizada até o número de 70 aminoácidos. A partir desse número considera-se que o composto formado é uma proteína. |
Aminoácidos essenciais e naturais
Todos os seres vivos produzem proteínas. No entanto, nem todos produzem os vinte tipos de aminoácidos necessários para a construção das proteínas. O homem, por exemplo, é capaz de sintetizar no fígado apenas onze dos vinte tipos de aminoácidos. Esses onze aminoácidos são considerados naturais para a nossa espécie. São eles:alanina, asparagina,cisteína, glicina, glutamina, histidina, prolina, tiroxina, ácido aspártico, ácido glutâmico.
Os outros nove tipos, os que não sintetizamos, são os essenciais e devem ser obtidos de quem os produz (plantas ou animais). São eles: arginina, fenilalanina, isoleucina, leucina, lisina, metionina, serina, treonina, triptofano e valina.
É preciso lembrar que um determinado aminoácido pode ser essencial para uma espécie e ser natural para outra.
Uma visão espacial da proteína
Uma molécula de proteína tem, a grosso modo, formato de um colar de contas. O fio fundamental da proteína, formado como uma seqüência de aminoácidos (cuja seqüência é determinada geneticamente), constitui a chamada estrutura primária da proteína.
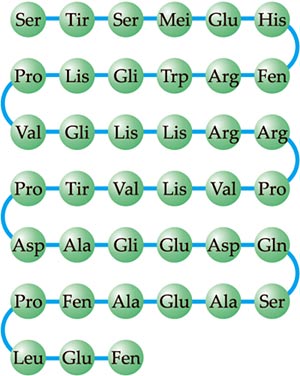
Ocorre, porém, que o papel biológico da maioria das proteínas depende de uma forma espacial muito mais elaborada. Assim, o fio fundamental é capaz de se enrolar sobre si mesmo, resultando um filamento espiralado que conduz à estrutura secundária, mantida estável por ligações que surgem entre os aminoácidos.
Novos dobramentos da espiral conduzem a uma nova forma, globosa, mantida estável graças a novas ligações que ocorrem entre os aminoácidos. Essa forma globosa representa a estrutura terciária.
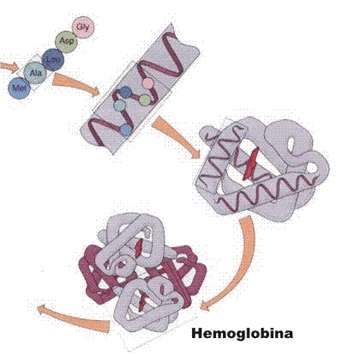
Em certas proteínas , cadeias polipeptídicas em estruturas terciárias globosa unem-se, originando uma forma espacial muito complexa, determinante do papel bioquímico da proteína. Essa nova forma constitui a estrutura quaternária dessas proteínas.
A figura abaixo mostra as quatro estruturas da hemoglobina juntas. Q hemoglobina esta presente dentro os glóbulos vermelhos do sangue e seu papel biológico é ligar-se a moléculas de oxigênio, transportando-as a nossos tecidos.
O fio do telefone pode ilustrar bem a idéia das estruturas protéicas:
Forma e função: um binômio inseparável
Logo mais você compreenderá de que modo a estrutura espacial de uma proteína está relacionado à função biológica que ela exerce. Por enquanto, lembre-se que, a manutenção das estruturas secundárias e terciárias deve-se a ligações que ocorrem entre os aminoácidos no interior da molécula protéica, determinando os diferentes aspectos espaciais observados.
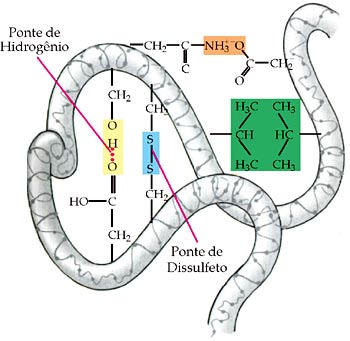
O aquecimento de uma proteína a determinadas temperaturas promove a ruptura das ligações internas entre os aminoácidos, responsáveis pela manutenção das estruturas secundária e terciária. Os aminoácidos não se separam, são se rompem as ligações peptídicas, porém a proteína fica “desmantelada”, perde a sua estrutura original. Dizemos que ocorreu uma desnaturação protéica, com perda da sua forma origina. Dessa maneira a função biológica da proteína é prejudicada.
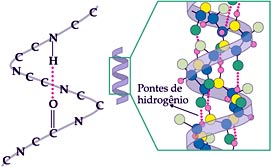
Nem sempre, porém, é a temperatura ou a alteração da acidez do meio que provoca a mudança da forma da proteína. Muitas vezes, a substituição de um simples aminoácido pode provocar alteração da forma da proteína.
Um exemplo importante é a substituição, na molécula de hemoglobina, do aminoácido ácido glutâmico pelo aminoácido valina. Essa simples troca provoca uma profunda alteração na forma da molécula inteira de hemoglobina, interferindo diretamente na sua capacidade de transportar oxigênio. Hemácias contendo a hemoglobina alterada adquirem o formato de foice, quando submetidas a certas condições, o que deu nome a essa anomalia: anemia falciforme. | 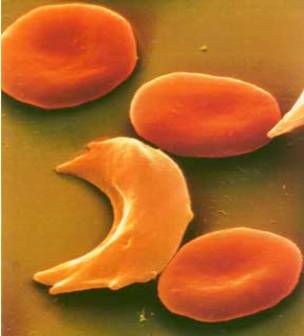 |
Enzimas
A vida depende da realização de inúmeras reações químicas que ocorrem no interior das células e também fora delas (em cavidades de órgãos, por exemplo). Por outro lado, todas essas reações dependem, para a sua realização , da existência de uma determinada enzima. As enzimas são substâncias do grupo das proteínas e atuam como catalisadores de reações químicas.
Catalisador é uma substância que acelera a velocidade de ocorrência de uma certa reação química.
Muitas enzimas possuem, além da porção protéica propriamente dita, constituída por uma seqüência de aminoácidos, uma porção não-protéica. A parte protéica é a apoenzima e a não protéica é o co-fator. Quando o co-fator é uma molécula orgânica, é chamado de coenzima. O mecanismo de atuação da enzima se inicia quando ela se liga ao reagente, mais propriamente conhecido como substrato. É formado um complexo enzima-substrato, instável, que logo se desfaz, liberando os produtos da reação a enzima, que permanece intacta embora tenha participado da reação. | 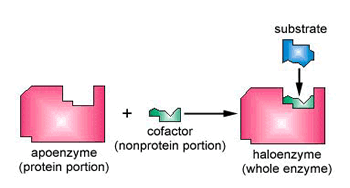 |
Mas para que ocorra uma reação química entre duas substâncias orgânicas que estão na mesma solução é preciso fornecer uma certa quantidade de energia, geralmente, na forma de calor, que favoreça o encontro e a colisão entre elas. A energia também é necessária para romper ligações químicas existentes entre os átomos de cada substância, favorecendo, assim a ocorrência de outras ligações químicas e a síntese de uma nova substância a partir das duas iniciais.
Essa energia de partida, que dá um “empurrão” para que uma reação química aconteça, é chamada de energia de ativação e possui um determinado valor.
A enzima provoca uma diminuição da energia de ativação necessária para que uma reação química aconteça e isso facilita a ocorrência da reação.
O mecanismo “chave-fechadura”
Na catálise de uma reação química, as enzimas interagem com os substratos, formando com eles, temporariamente, o chamado complexo enzima-substrato. Na formação das estruturas secundária e terciária de uma enzima (não esqueça que as enzimas são proteínas), acabam surgindo certos locais na molécula que servirão de encaixe para o alojamento de um ou mais substratos, do mesmo modo que uma chave se aloja na fechadura.
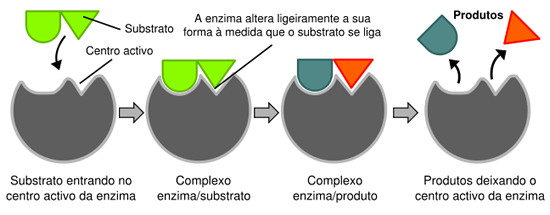
Esses locais de encaixe são chamados de sítio ativos e ficam na superfície da enzima. Ao se encaixarem nos sítios ativos, os substratos ficam próximos um do outro e podem reagir mais facilmente.
Assim que ocorre a reação química com os substratos, desfaz-se o complexo enzima-substrato. Liberam-se os produtos e a enzima volta a atrair novos substratos para a formação de outros complexos.
Lembre-se!! Uma enzima não é consumida durante a reação química que ela catalisa.
Fatores que afetam a atividade das enzimas
Temperatura
A temperatura é um fator importante na atividade das enzimas. Dentro de certos limites, a velocidade de uma reação enzimática aumenta com o aumento da temperatura. Entretanto, a partir de uma determinada temperatura, a velocidade da reação diminui bruscamente.
O aumento de temperatura provoca maior agitação das moléculas e, portanto, maiores possibilidades de elas se chocarem para reagir. Porém, se for ultrapassada certa temperatura, a agitação das moléculas se torna tão intensa que as ligações que estabilizam a estrutura espacial da enzima se rompem e ela se desnatura.
Para cada tipo de enzima existe uma temperatura ótima, na qual a velocidade da reação é máxima, permitindo o maior número possível de colisões moleculares sem desnaturar a enzima. A maioria das enzimas humanas, têm sua temperatura ótima entre 35 e 40ºC, a faixa de temperatura normal do nosso corpo. Já bactéria que vivem em fontes de água quente têm enzimas cuja temperatura ótima fica ao redor de 70ºC.
Grau de acidez (pH)
Outro fator que afeta a forma das proteínas é o grau de acidez do meio, também conhecido como pH (potencial hidrogeniônico). A escala de pH vai de 0 a 14 e mede a concentração relativa de íons hidrogênio (H+) em um determinado meio. O valor 7 apresenta um meio neutro, nem ácido nem básico. Valores próximos de 0 são os mais ácidos e os próximos de 14 são os mais básicos (alcalinos).
Cada enzima tem um pH ótimo de atuação, no qual a sua atividade é máxima. O pH ótimo para a maioria das enzimas fica entre 6 e 8, mas há exceções. A pepsina, por exemplo, uma enzima digestiva estomacal, atua eficientemente no pH fortemente ácido de nosso estômago (em torno de 2), onde a maioria das enzimas seria desnaturada. A tripsina, por sua vez, é uma enzima digestiva que atua no ambiente alcalino do intestino, tendo um pH ótimo situado em torno de 8.
As proteínas e nossa alimentação

O desenvolvimento saudável de uma criança depende do fornecimento de proteína de qualidade. Por proteínas de qualidade entende-se as que possuem todos os aminoácidos essenciais para a nossa espécie. A maturação cerebral depende do fornecimento correto, na idade certa, das proteínas de alto valor nutritivo. Pobreza de proteínas na infância acarreta sérios problemas de conduta e raciocínio na fase adulta.
A doença conhecida como Kwashiorkor, em que a criança apresenta a abdômen e membros inchados, alteração na cor dos cabelos e precário desenvolvimento intelectual, é uma manifestação de deficiência protéica na infância e mesmo em adultos.
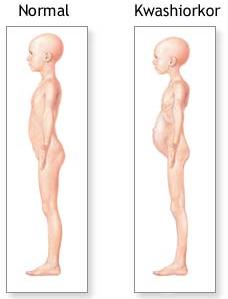
As autoridades mundiais estão cada vez mais preocupadas com a correta alimentação dos povos que, normalmente, não possuem acesso fácil aos alimentos protéicos.
Em muitas regiões do mundo, as pessoas recorrem aos alimentos ricos em carboidratos (excelentes substâncias fornecedoras de energia), porém pobre em aminoácidos.
Elas engordam, mas apresentam deficiência em proteínas. O ideal é incentivar o consumo de mais proteínas e obter, assim, um desenvolvimento mais saudável do organismo.
As proteínas mais "saudáveis", de melhor qualidade, são as de origem animal. As de maior teor em aminoácidos essenciais são encontradas nas carnes de peixe, de vaca, de aves e no leite.
Um aspecto importante a ser considerado no consumo de cereais, é que eles precisam ser utilizados sem ser beneficiados. No arroz, sem casca e polido, o que sobra é apenas o amido, e o mesmo ocorre com os grãos de trigo no preparo da farinha. Deve-se consumir esses alimentos na forma integral, já que as proteínas são encontradas nas películas que recobrem os grãos. Mais recentemente tem se incentivado o consumo de arroz parbolizado (do inglês, parboil = ferventar), isto é, submetido a um processo em que as proteínas da película interna à casca aderem ao grão. Outra grande fonte de proteínas é a soja e todos os seus derivados.
Ácidos nucléicos
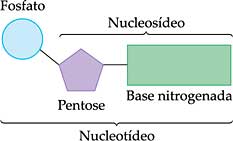
Os ácidos nucléicos são moléculas gigantes (macromoléculas), formadas por unidades monoméricas menores conhecidas como nucleotídeos. Cada nucleotídeo, por sua vez, é formado por três partes:
- um açúcar do grupo das pentoses (monossacarídeos com cinco átomos de carbono);
- um radical “fosfato”, derivado da molécula do ácido ortofosfórico (H3PO4).
- uma base orgânica nitrogenada.
Sabia-se de sua presença nas células, mas a descoberta de sua função como substâncias controladoras da atividade celular foi um dos passos mais importantes da história da Biologia. A partir do século XIX, com os trabalhos do médico suíço Miescher, iniciaram-se as suspeitas de que os ácidos nucléicos eram os responsáveis diretos por tudo o que acontecia em uma célula. Em 1953, o bioquímico norte-americano James D. Watson e o biologista molecular Francis Crick propuseram um modelo que procurava esclarecer a estrutura e os princípios de funcionamento dessas substâncias.

O volume de conhecimento acumulados a partir de então caracteriza o mais extraordinário conhecimento biológico que culminou, nos dias de hoje, com a criação da Engenharia Genética, área da Biologia que lida diretamente com os ácidos nucléicos e o seu papel biológico.
De seus três componentes (açúcar, radical fosfato e base orgânica nitrogenada) apenas o radical fosfato não varia no nucleotídeo. Os açucares e as bases nitrogenadas são variáveis.
Quanto aos açucares, dois tipos de pentoses podem fazer parte de um nucleotídeo: ribose e desoxirribose (assim chamada por ter um átomo de oxigênio a menos em relação à ribose.
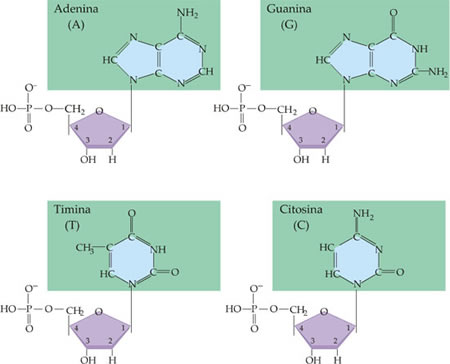
Já as bases nitrogenadas pertencem a dois grupos:
- as púricas: adenina (A) e guanina (G);
- as pirimídicas: timina (T), citosina (C) e uracila (U).
DNA e RNA: Qual é a diferença?
É da associação dos diferentes nucleotídeos que se formam as macromoléculas dos dois tipos de ácidos nucléicos: o ácido ribonucléico (RNA) e o ácido desoxirribonucléico (DNA). Eles foram assim chamados em função dos açúcar presente em suas moléculas: O RNA contém o açúcar ribose e o DNA contém o açúcar desoxirribose.
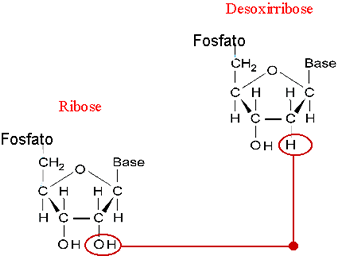
Outra diferença importante entre as moléculas de DNA e a de RNA diz respeito às bases nitrogenadas: no DNA, as bases são citosina, guanina, adenina e timina; no RNA, no lugar da timina, encontra-se a uracila. A importância e o funcionamento dos ácidos nucléicos.
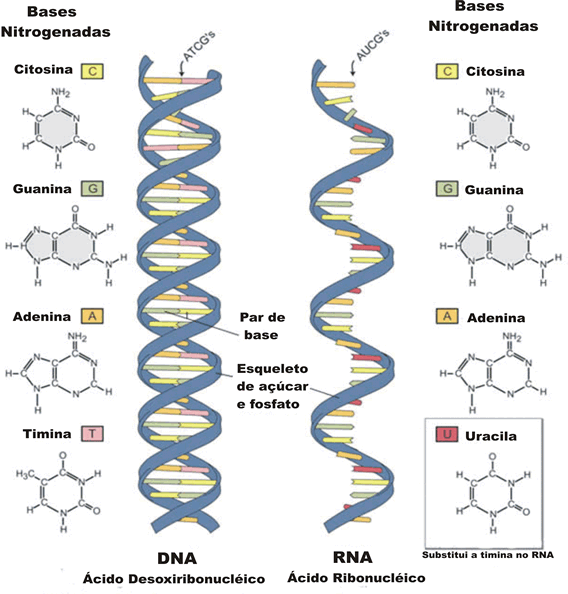
Fonte: www.sobiologia.com
Atividades 1
1. Cite as principais funções dos carboidratos.
2. Indique as características e principais funções de cada um dos polissacarídeos:
a) Amido
b) Glicogênio.
c) Celulose
3. O que são monossacarídeos e quais são os mais comuns?
4. O que são dissacarídeos? Dê exemplos.
5. Cite três funções dos lipídio no organismo humano.
6. Quais são as duas unidades básicas formadoras dos lipídios?
7. Dê cinco exemplos de lipídios.
8. O que são HDL e LDL e qual a importância dos dois na saúde do ser humano?
9. Para evitar o colesterol podemos trocar simplesmente a gordura animal pelos óleos vegetais? Por quê?
Atividades 1
1. Cite as principais funções dos carboidratos.
2. Indique as características e principais funções de cada um dos polissacarídeos:
a) Amido
b) Glicogênio.
c) Celulose
3. O que são monossacarídeos e quais são os mais comuns?
4. O que são dissacarídeos? Dê exemplos.
5. Cite três funções dos lipídio no organismo humano.
6. Quais são as duas unidades básicas formadoras dos lipídios?
7. Dê cinco exemplos de lipídios.
8. O que são HDL e LDL e qual a importância dos dois na saúde do ser humano?
9. Para evitar o colesterol podemos trocar simplesmente a gordura animal pelos óleos vegetais? Por quê?
Atividade 2
1. O que são proteínas e qual a sua função no corpo humano?
2. Como os aminoácidos se unem para formar as proteínas? Como se chama essa ligação?
3. Qual a estrutura molecular de um aminoácido?
4. Cite duas funções básicas da proteína no organismo humano.
5. O que são aminoácidos naturis e eswsenciais e onde eles são encontrados?
6. Quanto a forma estrutural, como podemos classificar as proteína?
7. O que é uma desnaturação de uma proteína e em que condições ela pode ocorrer?
8. Cite um exemplo em que a substituição de um aminoácido na proteína provoca uma alteração e a doença ema causa nos seres humanos.
ATIVIDADES - ENZIMAS
1. Qual a importânica das enzimas em relação aos seres vivos?
2. O que são enzimas?
3. O que é uma substância catalizadora?
4. De que é composta uma enzima?
5. O que significa o mecanismo chave fechadura em uma enzima?
6. O que é energia de ativação?
7. Explique os fatores que interferem no funcionamento de uma enzimas.
ATIVIDADES - ENZIMAS
1. Qual a importânica das enzimas em relação aos seres vivos?
2. O que são enzimas?
3. O que é uma substância catalizadora?
4. De que é composta uma enzima?
5. O que significa o mecanismo chave fechadura em uma enzima?
6. O que é energia de ativação?
7. Explique os fatores que interferem no funcionamento de uma enzimas.

gostei muito desse site, por que nos dá mais informações do que realmente prescisamos.È muito amplo, com ótimas imagens e bem organizado. Parabéns Júlio Ramos!!!!!!!!!!!
ResponderExcluir